
2025年5月,吉美瑞生集团(Regend Therapeutics)的全资子公司上海吉锐医学科技有限公司自主研发的自体肾前体细胞回输制剂(吉美瑞生“REGEND003”)的新药注册临床试验I/II期申请,已顺利获得国家药品监督管理局NMPA批准(受理号:CXSL2500196),用于治疗2型糖尿病合并慢性肾脏疾病(CKD)。这是吉美瑞生集团基于其自主知识产权的“R-Clone”技术平台获得国家药品监督管理局批准的第三款细胞治疗1类新药临床试验批件。
据国家药品监督管理局药品审评中心官网公布,吉美瑞生旗下全资子公司上海吉锐医学科技有限公司的REGEND003细胞自体回输制剂,于2025年5月27日获得药监局颁发的《药物临床试验批准通知书》(受理号:CXSL2500196)。这款由吉美瑞生自主研发的全球首创干细胞新药是首个获批进入临床的肾脏干细胞产品,利用自体肾脏来源的SOX9+CD73+肾前体细胞(一种肾脏干细胞)肾内移植策略,可实现肾脏组织的再生修复及功能重建,在多种慢性肾脏疾病治疗中具有巨大的潜力。
慢性肾脏疾病(CKD)作为威胁全球1.3亿糖尿病患者的严重并发症,以不可逆的肾功能损伤为特征,约27.1%~83.6%的糖尿病患者伴随肾脏损害,临床表现为持续性蛋白尿及肾小球滤过率(GFR)进行性下降,最终可能发展为终末期肾病(ESRD),依赖透析或肾移植生存。现有疗法如SGLT2抑制剂、血糖/血压控制或透析虽能延缓病情进展,但无法逆转肾单位损失或促进组织修复。尤其对于中晚期CKD患者,长期透析不仅生活质量显著降低,还伴随心血管并发症等高风险,而肾移植则面临供体短缺和免疫排斥的挑战。大量患者在漫长的治疗过程中,承受着身体与经济的双重压力。因此亟待一种能够修复肾脏损伤、延缓甚至逆转疾病进展的创新疗法,以填补这一关键临床空白。
本次获批的REGEND003细胞自体回输制剂(即肾前体细胞疗法)通过突破性再生技术破解治疗困局。该干细胞药物从患者尿液中无创提取具有再生功能的SOX9+CD73+肾前体细胞,经体外扩增后回输至肾脏损伤区域,通过分化和旁分泌两种途径协同,实现肾小管及肾小球组织细胞的功能性再生,从而修复肾脏结构,提升肾脏功能。
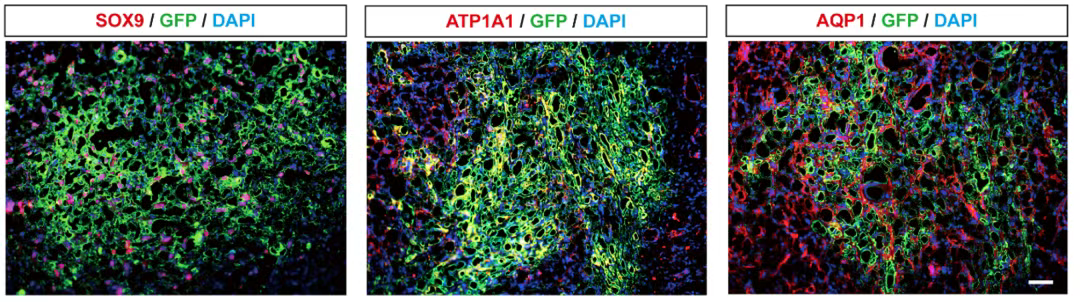
肾内移植的SOX9+CD73+人肾脏前体细胞
目前美国FDA已批准Rilparencel靶向肾内给药治疗糖尿病肾病的III期临床试验,有望在明年实现上市应用。已披露的II期临床显示,Rilparencel细胞治疗在总体上具有良好的安全性和有效性。主要终点指标eGFR年下降率从注射前−4.63 mL/min/1.73m²减缓至注射后−1.69 mL/min/1.73m²(p=0.015),有32%的患者在治疗后eGFR出现提升。然而,Rilparencel需肾脏活检取样,取样过程容易造成针对肾脏的创伤,且仅能采样一次,培养终产品为多种复合细胞群体的混合物,有效成分纯度不明确、可能存在潜在个体疗效差异。与之相比,吉美瑞生的REGEND003肾前体细胞产品来源于尿液,取样过程完全无创,可多次重复采样,最终产品为高纯度的自体肾前体细胞,有效成分纯度更高、所需剂量更小,可预见的术后不良反应更为可控,有望带来疗效的进一步提升。
REGEND003注册临床I/II期试验负责人、同济大学附属同济医院肾脏内科主任、上海市医师协会肾脏医师分会副会长余晨教授表示:“很高兴能见证一款针对慢性肾病的全新干细胞药物能够得到药监局的认可获批。中国慢性肾病患者基数大、医疗负担沉重,干细胞治疗为患者带来了新的希望。我们将联合全国多家高水平专业医疗机构,规范开展高质量的多中心临床试验,探索干细胞药物的有效性和安全性,期待早日为患者健康提供更好的医疗服务。”
吉美瑞生科学创始人、同济大学左为教授表示:“团队从2017年开始立项启动了基于成体干细胞的肾脏再生技术研发,期间获得了两项国家重点研发计划干细胞专项的资助,与同济大学附属同济医院、解放军总医院、同济大学附属东方医院、南方医院等科研及临床团队开展了紧密合作,发表了一系列高影响力的学术论文。历经“八年磨一剑”,终于迈出了基础科学成果向临床产业转化的步伐。期待能在后续临床试验中对REGEND003的安全性和有效性完成全面的评估,从而开发出继REGEND003气道基底层干细胞产品之后,又一再生医学产品的重磅成果。”
吉美瑞生参照国际标准与国内法规,已完成REGEND003细胞自体回输制剂安全性验证、有效性研究、质量管控体系搭建及规模化生产筹备。待药物临床试验启动,吉美瑞生将即刻开展受试者招募工作,通过严格筛选流程确定符合标准的受试者,并以标准化操作流程确保试验科学规范。后续,吉美瑞生还将联合同济大学附属同济医院团队,在保障药物安全有效的前提下,加速推进REGEND003细胞自体回输制剂的研发与应用落地,致力于填补临床空白,为患者带来新希望。
想要解锁更多药品信息吗?查询yl23455永利官网(原药融云)数据库(vip.sdbaichao.com/?zmt-mhwz)掌握药企公司基本信息、投融资情况、产品管线分布、药物销售情况与各维度分析、药物研发情况、年度报告、最新进展动态、临床试验信息、市场规模与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!












































 浙公网安备33011002015279
浙公网安备33011002015279
 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论